


(감동) 2200원짜리 피자(4분 20초)


• 전자 간 반발력을 최소로 하기 위한 배열로 분자 구조가 이루어짐을 설명할 수 있다.
• 분자 구조에 따른 물질의 특성과 기능의 차이점을 설명할 수 있다.


다음의 그림 자료를 보고 비활성 기체들의 공통적인 특성을 탐구해 보자

헬륨 : 기구 네온 : 네온사인 아르곤 : LED
그림 I-28 비활성 기체의 이용
![]()
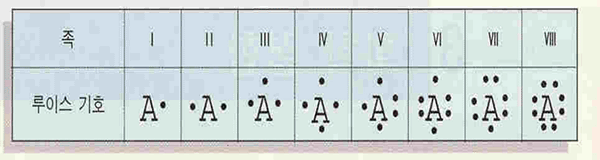
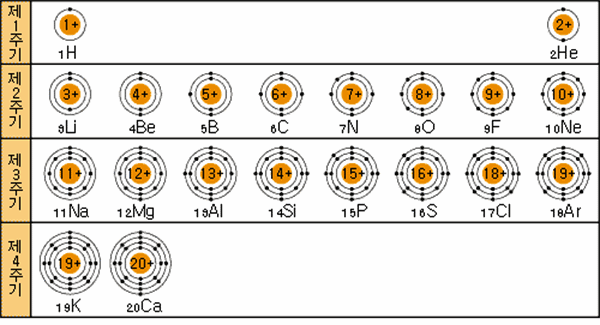
그림 I-29 전형 원소의 전자 배치

1. 다음 원자들이 옥텟 규칙에 따라 생성될 수 있는 이온을 기호로 나타내시오.
1) 마그네슘(Mg)
2) 산소(O)
3) 칼륨(K)
4) 황(S)

혼자 있는 것 보다 둘이 있으면 더 편안하고 안정적입니다. 남자와 여자가 결혼을 하듯 양이온과 음이온이 서로 끌리는 힘에 의해 이온 결합을 합니다.

다음은 염화나트륨을 형성하는 모형을 나타낸 그림이다. 나트륨(Na)과 염소(Cl2)가 결합할 때, 이들 사이에 일어나는 변화를 탐구해 보자.
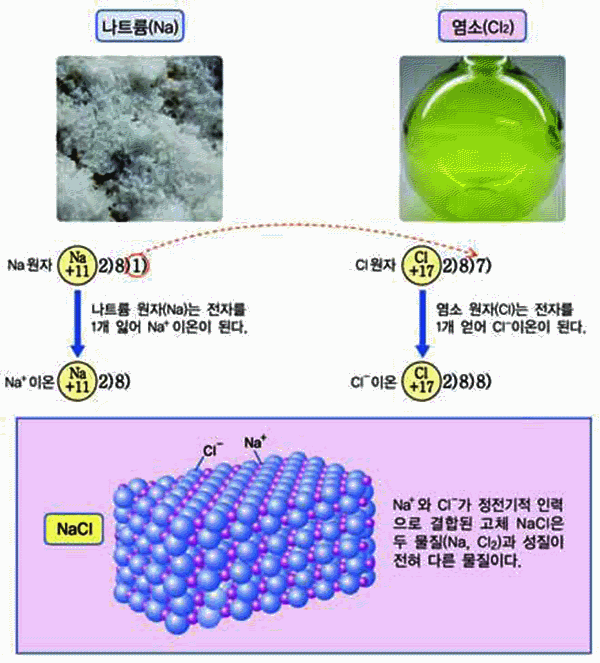
그림 I-30 NaCl의 형성 과정
![]()
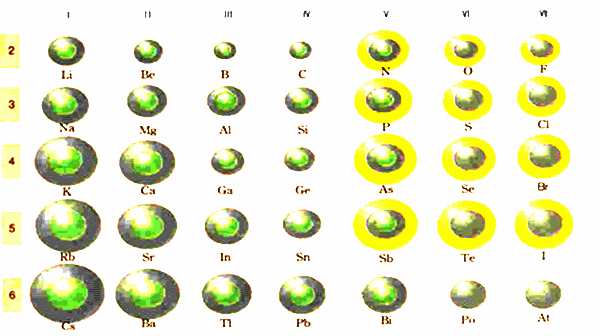
그림 I-31 이온의 크기
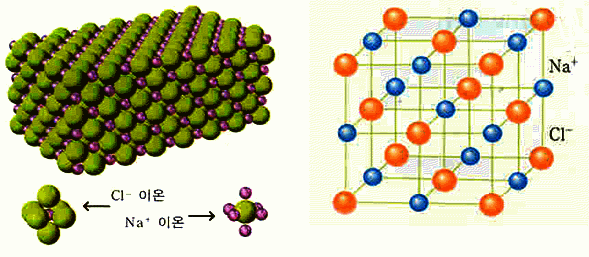
그림 I-32 염화나트륨의 모형
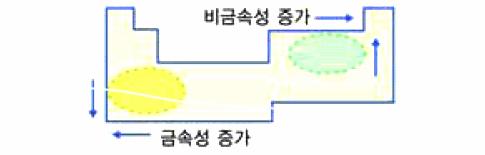
그림 I-33 이온 결합을 이루는 원자
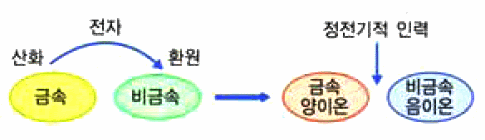
그림 I-34 이온 결합 형성 모형
![]()
이온 결합물의 화학식 표시법
Xa + Yb → XbYa

2. 다음 이온들이 결합하여 생성되는 이온 결합 물질을 화학식으로 써 보자.
1) Na+과 F-
2) K+과 NO3 -
3) Mg2+과 Cl-
4) Al3+과 O2-
3. 칼륨(K)과 나트륨(Na) 사이에 이온 결합이 형성되지 않는 이유는 무엇일까?


전자를 얻거나 잃는 정도가 비슷한 원자들은 각 원자가 가진 전자쌍을 공유하는 공유결합을 합니다

다음은 비금속을 나타내는 수소(H) 입자들의 만남을 모형으로 나타낸 그림 이다. 이들 사이에 일어나는 변화를 탐구해 보자.
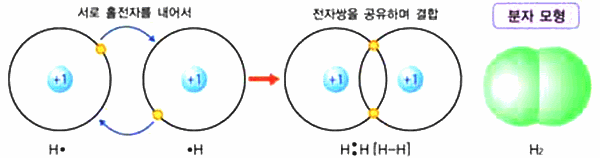
그림 I-35 H2의 공유 결합 모형
![]()
![]()
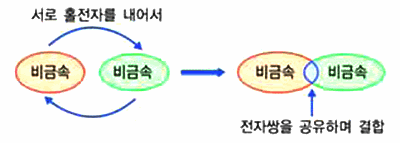
그림 I-36 공유 결합 형성 과정
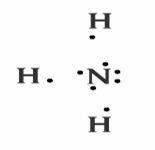
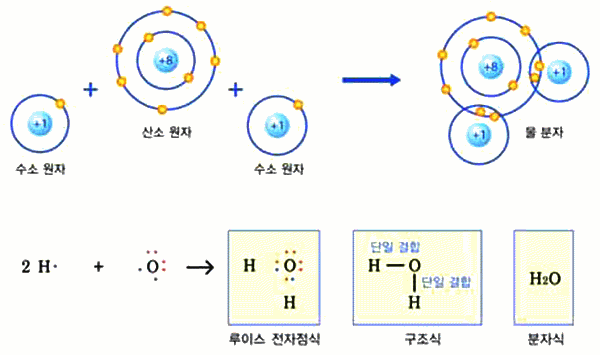
그림 I-37 공유 결합으로 이루어진 물분자의 형성 과정과 표현 방법
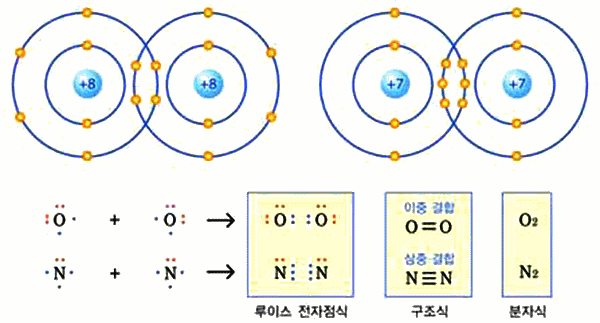
그림 I-38 공유 결합으로 이루어진 O2, N2의 모형과 표현 방법
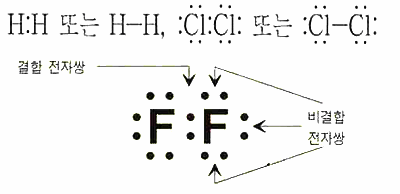
![]()
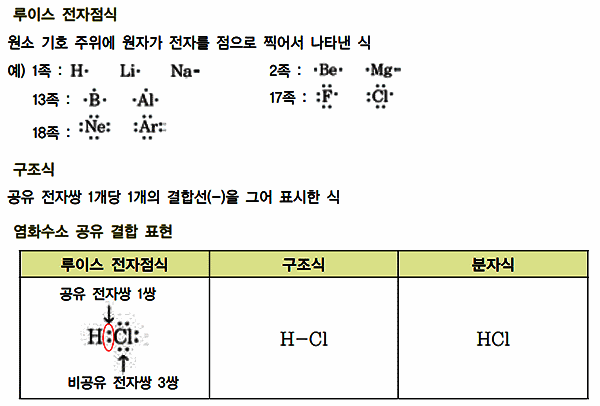

4. 다음 분자들을 루이스 전자점식, 구조식, 분자식으로 나타내시오.
1) H2O
2) CO2
3) NH3
4) BF3
5) H2S
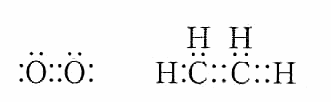
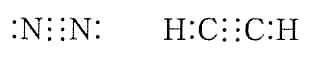
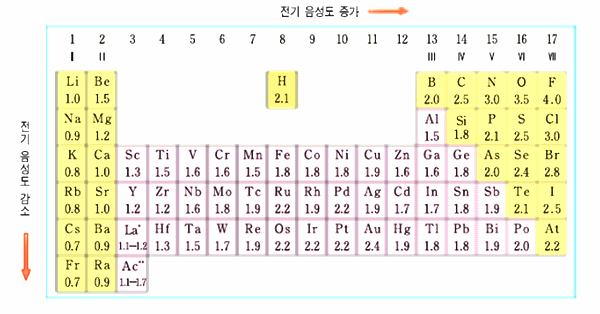
그림 I-38 전기 음성도
